2026年1月22日,我院吴亚红团队在多肽抗肿瘤方面取得进展,相关成果《Development of a lymph node-homing peptide vaccine targeting C-C chemokine receptor 7-positive dendritic cells with enhanced antitumor immunity》在线发表在国际期刊《Journal of Controlled Release》(中科院1区TOP期刊,IF:11.5)。郑州大学生命科学学院的庞丽薇博士为论文的唯一一作,郑州大学生命科学学院吴亚红副教授和中山大学药学院高艳锋教授为论文的共同通讯作者,郑州大学生命科学学院为第一作者单位。
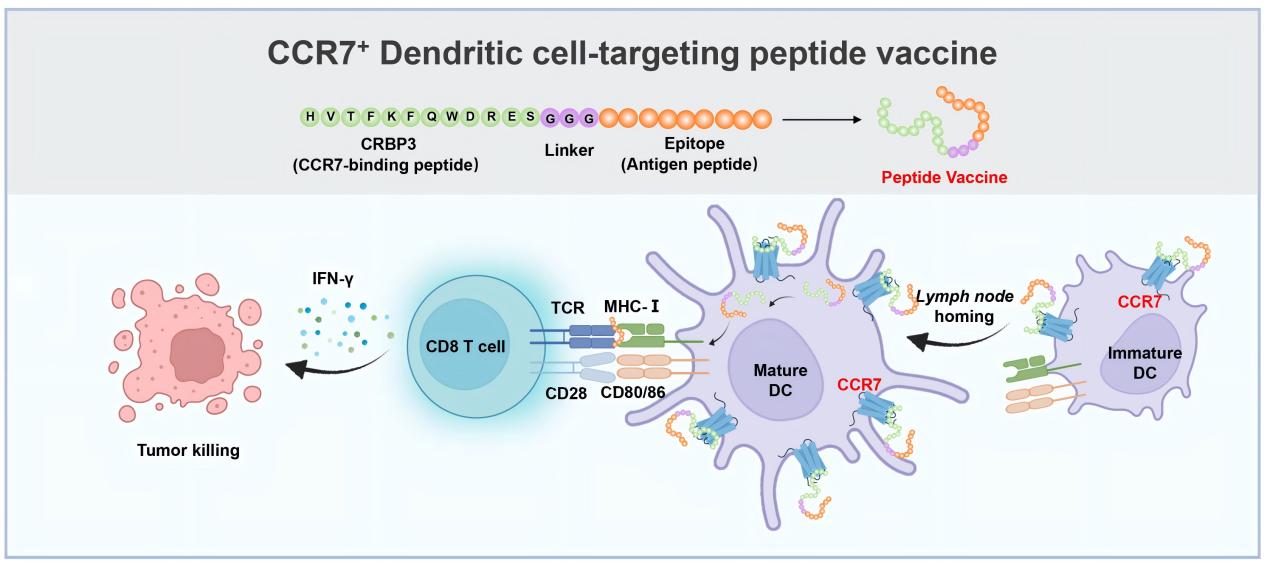
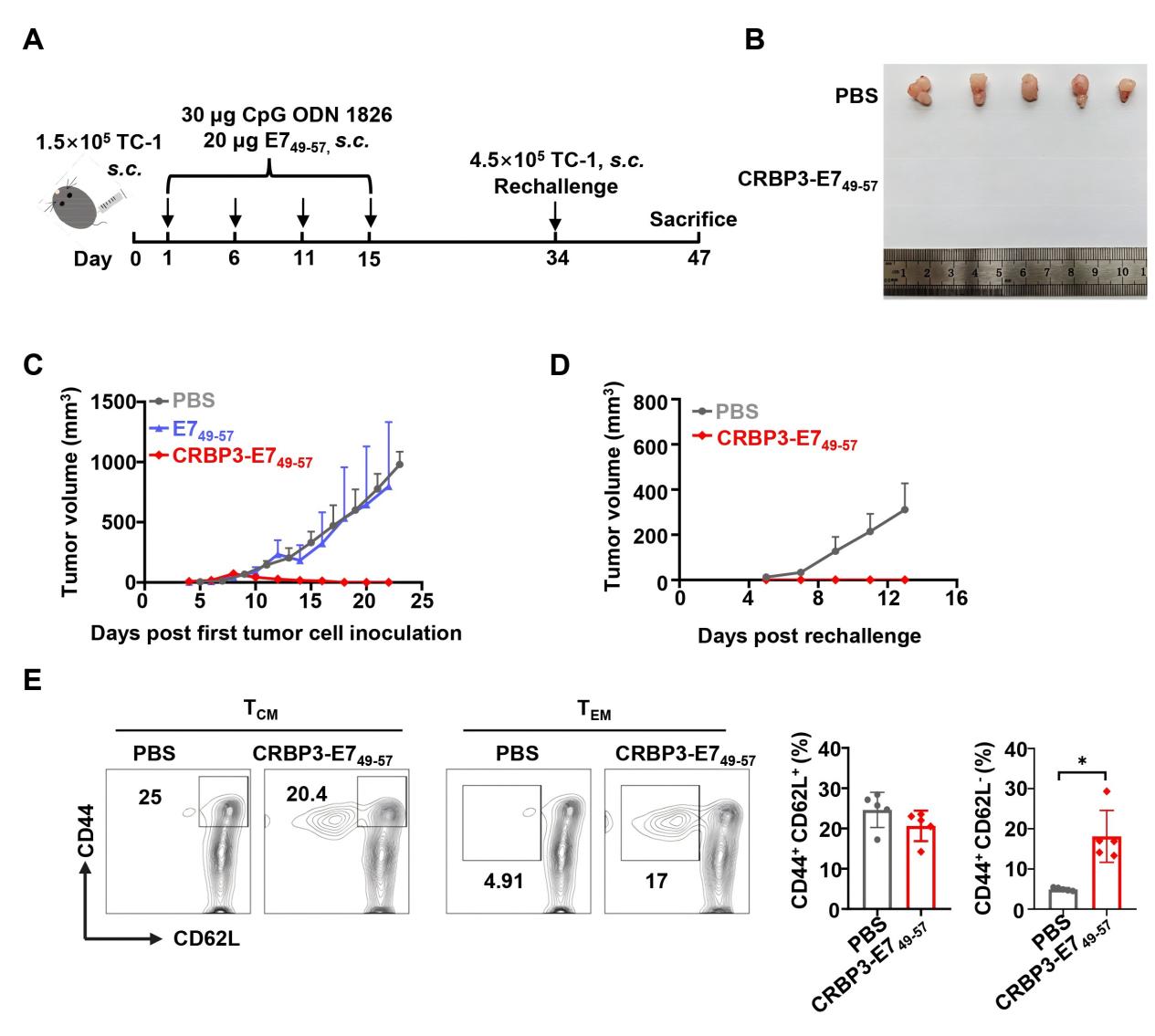
肿瘤多肽疫苗临床应用的最大问题是疫苗的靶向性以及体内激活CD8+T细胞的效果不佳,这也是绝大多数肿瘤多肽疫苗临床失败的主要原因。为了解决这一问题,通过表面受体特异性靶向专职性抗原提呈细胞—树突状细胞是一种有前景的策略。CCR7,一种趋化因子受体,在树突状细胞的迁移和淋巴结归巢中发挥着至关重要的作用,成为开发靶向树突状细胞免疫疗法的理想靶点。在本研究中,通过噬菌体展示肽库技术和亲和实验,课题组筛选获得一条能够特异性靶向CCR7的多肽CRBP3。在体外实验中,CRBP3能够高效亲和及被未成熟和成熟的树突状细胞内吞。在小鼠足垫部位注射后,CRBP3能够有效积聚到腘窝淋巴结中。当CRBP3与抗原表位肽OVA257-264偶联时,无论树突状细胞是否成熟,偶联肽疫苗(CRBP3-OVA257-264)均能显著增强树突状细胞表面的第一信号—抗原肽/ MHC-I复合物的形成,并显著促进抗原特异性CD8+T细胞的增殖以及IFN-γ+CD8+T细胞的比例。体内抗肿瘤活性实验结果显示,CRBP3与外源性抗原肽OVA257-264和内源性抗原肽HPV16 E749-57偶联后,分别在抗PD-1响应性的B16-OVA小鼠模型和抗PD-1不响应的TC-1肿瘤模型中展现出显著的抗肿瘤免疫应答。值得注意的是,CRBP3-E749-57偶联肽疫苗在TC-1肿瘤模型中诱导了肿瘤的完全消退,并且在三倍荷瘤细胞的再挑战时仍能提供持久的保护,抑制肿瘤的发生。该工作证明了靶向CCR7能够显著增强肿瘤多肽疫苗的体内抗肿瘤免疫应答,表明CCR7靶向肽可以作为一种多功能的工具用于开发淋巴结靶向的癌症免疫疗法。该研究得到了国家自然科学基金面上项目,河南省优秀青年基金项目等基金的支持。